We use cookies to improve and analyse your browsing experience on our web. You can accept these cookies, reject them or choose your settings by clicking on the corresponding buttons. Please note that rejecting cookies may affect your browsing experience. For more information you can consult our Cookies policy.
Cookies are an essential part of how our web works. The main goal of cookies is to make your browsing experience more comfortable and efficient and to improve our services and the web itself.
Here you can find all the information about the cookies we use and you can activate and/or deactivate them according to your preferences, except for those cookies that are strictly necessary for the operation of the web. Blocking some cookies may affect your experience on the web and how the site works. For more information you can visit our Cookie Policy.
These Cookies are necessary for the web to function and cannot be disabled on our systems. They are generally only set up in response to actions you may take such as requesting services, setting your privacy preferences, logging in or completing forms. You can set your browser to block or warn you about these cookies, but some parts of the web will not work. Information about Cookies.
These Cookies allow us to count the number of visits and traffic sources so that we can measure and improve the performance of our site. They help us to find out which pages are the most popular and least popular, and to see how visitors move around the web. All information collected by these Cookies is aggregated and therefore anonymous. If you do not allow these Cookies we will not know when you visited our web. Information about Cookies.
These cookies are used to analyse your activity in order to show you personalised advertisements.Information about Cookies.
Change theme

Revision mode

Habrás visto muchas veces cómo se derrite un cubito de hielo una vez que lo sacas del congelador. Para conseguirlo, lo único que necesitamos es suministrarle calor (aunque no seamos conscientes de ello, le estamos sometiendo al calor de la habitación, cuya temperatura es mayor que la del congelador). En cambio, si lo que queremos es hacer cubitos de hielo, lo más fácil es poner agua líquida en una cubitera y dejarla un tiempo en el congelador, es decir, enfriarla.
En ambos casos estamos pasando de un estado de la materia a otro, lo que conocemos como cambios de estado.
Dado que los estados de agregación de la materia están relacionados con la disposición de sus partículas constituyentes, los cambios de estado supondrán una modificación de dicha disposición, pero nunca del tipo de partícula (de ahí que la sustancia continúe siendo la misma).
Todas las sustancias pueden encontrase en los tres estados de la materia y pasar de uno a otro con solo modificar la temperatura. Sin embargo, hay sustancias, como el oxígeno, que solo conocemos en un estado, en este caso el gaseoso. ¿No es esto contradictorio? En absoluto. En el caso del oxígeno, lo que ocurre es que necesitaríamos alcanzar temperaturas muy bajas para poder observarlo en estado tanto líquido como sólido. Sería necesaria una temperatura inferior a –183 °C para conseguir oxígeno líquido, y menor de –218 °C para obtener oxígeno sólido. Estas temperaturas tan bajas no son habituales en la vida cotidiana, pero sí es posible alcanzarlas en los laboratorios.
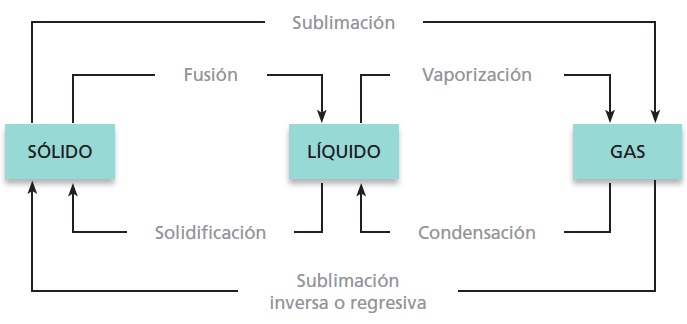
En el siguiente esquema se muestran los nombres de todos los cambios de estado:

Actividad 6
¿Encuentras alguna relación entre el cambio climático y el deshielo de los polos? Rellena los espacios en blanco.


El paso del estado sólido al líquido se denomina fusión. La temperatura a la que funden las sustancias no es igual para todas ellas, sino que depende de cada una. Por ejemplo, el hielo (agua sólida) funde a 0 °C a nivel del mar; sin embargo, el oro lo hace a 1063 °C.
El proceso contrario a la fusión es la solidificación (por tanto, el paso de líquido a sólido).
Por ejemplo, si introducimos un termómetro en un vaso de agua y lo ponemos en la ventana en un día muy frío en el que esté nevando, el agua no se transforma en hielo hasta que no alcanza los 0 °C. Si recuerdas, esta es la temperatura a la que funden los cubitos de hielo.
El paso del estado líquido al gaseoso se denomina vaporización, y puede producirse de dos formas diferentes:


El proceso contrario a la vaporización es la condensación, que es el paso de gas a líquido.
Actividad 7
Actividad 8
¿Qué relación hay entre la temperatura a la que funde una sustancia en estado sólido y la temperatura a la que solidifica esa misma sustancia?
Actividad 9
¿Es imprescindible que los líquidos hiervan para conseguir que pasen a estado gaseoso?
A medida que calentamos el hielo la temperatura comienza a subir poco a poco. Sin embargo, si nos fijamos bien, observaremos que el termómetro se mantendrá estable en dos momentos determinados en nuestro experimento:
Algo curioso que veremos es que, mientras duran los cambios de estado, la temperatura permanece constante y no vuelve a subir hasta que el cambio ha terminado (no queda absolutamente nada de hielo en el primer caso y nada de agua líquida en el segundo).
La temperatura a la que se produce cada cambio de estado será distinta para cada sustancia.

Esta representación gráfica temperatura-tiempo se conoce como gráfica de calentamiento.
Si en lugar de calentar enfriamos, obtendremos una gráfica similar, llamada gráfica de enfriamiento, que será descendente en lugar de ascendente.
Actividad 10
Construye la gráfica de enfriamiento del agua si partimos de vapor de agua a 130 °C y dejamos de enfriar a –10 °C.
Actividad 11
Razona, a partir de la gráfica del ejemplo, en qué estado de agregación se encontrará el agua a 50 °C y a 125 °C.
Actividad 12
Actividad 7
A nivel del mar, el hielo se derrite a 0 ºC. ¿Por qué crees que se hace referencia al nivel del mar? Investígalo y elige la respuesta correcta:
Actividad 10
Cuál de las siguientes gráficas representa el enfriamiento del agua si partimos de vapor de agua a 130 °C y dejamos de enfriar a –10 °C.
Actividad 12
Ordena, paso a paso, cóActividad 12 mo llevarías a cabo en el laboratorio el estudio experimental de los cambios de estado del agua.

